Was sind die genetischen Ursachen von SMA?
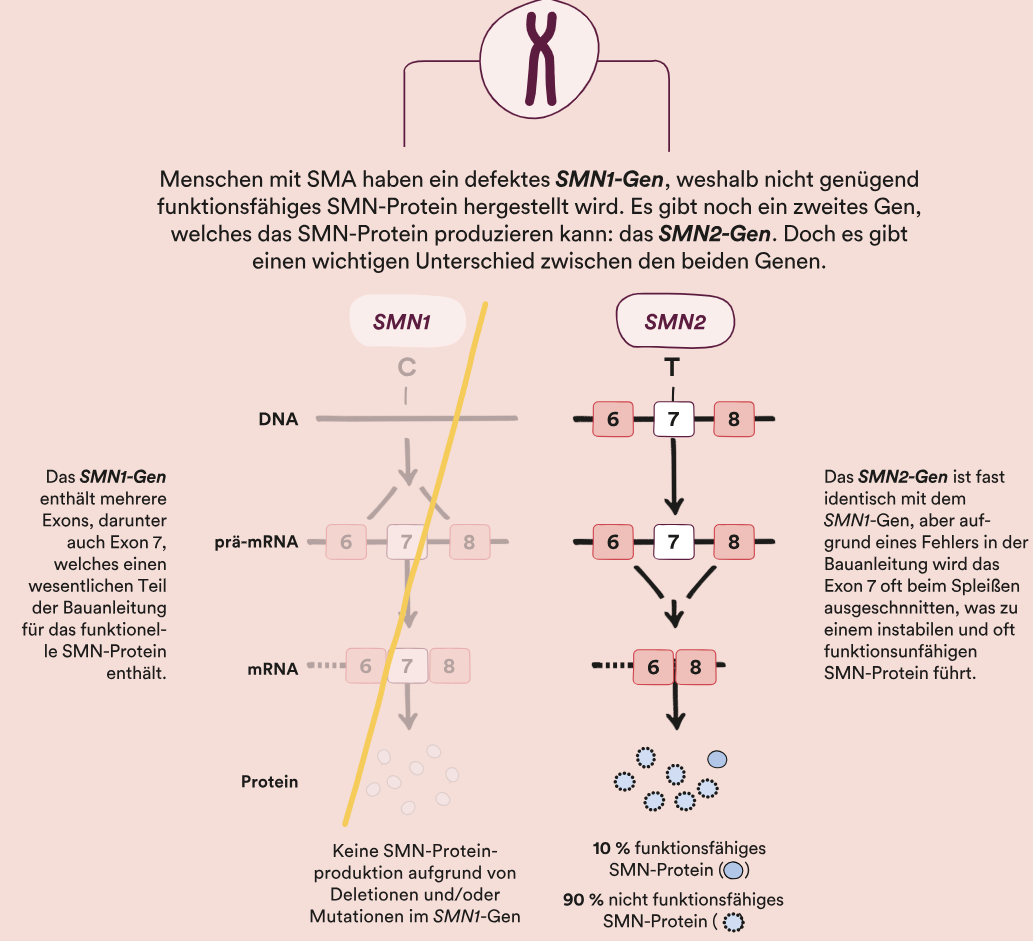
Spinale Muskelatrophie entsteht durch Veränderungen im SMN1-Gen, das entweder defekt ist oder vollständig fehlt. Dadurch wird nicht genügend funktionsfähiges Survival-of-Motoneuron-Protein (SMN-Protein) produziert. 1 Dieses Protein ist für das Überleben der Motoneuronen essenziell. 2 , 3 Der SMN-Mangel ist die Grundlage dafür, dass Therapien entweder die SMN-Proteinmenge erhöhen oder den Defekt genetisch beheben.
Neben SMN1 existiert das SMN2-Gen, das ebenfalls SMN-Protein herstellen kann – jedoch deutlich weniger effizient (siehe Abb. 1). 4-6